Aantal Protonen Neutronen En Elektronen
Weet je nog die lessen scheikunde waarin je leerde over atomen? Misschien dacht je toen: "Wanneer ga ik dit ooit in de praktijk gebruiken?" Maar de waarheid is, de kennis over atomen – en specifiek het aantal protonen, neutronen en elektronen – is fundamenteel voor het begrijpen van de wereld om ons heen. Van de manier waarop medicijnen werken tot de energie die onze huizen verlicht, alles is terug te voeren op deze kleine bouwstenen.
Laten we duiken in de wereld van de atomen en kijken waarom deze aantallen zo belangrijk zijn.
Waarom zijn Protonen, Neutronen en Elektronen Belangrijk?
Stel je voor: je bouwt een huis. De bakstenen, de fundering, de balken – elk element speelt een cruciale rol in de stevigheid en functionaliteit van het geheel. Protonen, neutronen en elektronen zijn de bouwstenen van atomen, en atomen zijn de bouwstenen van alle materie. De aantallen van deze deeltjes bepalen de eigenschappen van een element en hoe het zich gedraagt in chemische reacties.
Hier is een kort overzicht van de rol van elk deeltje:
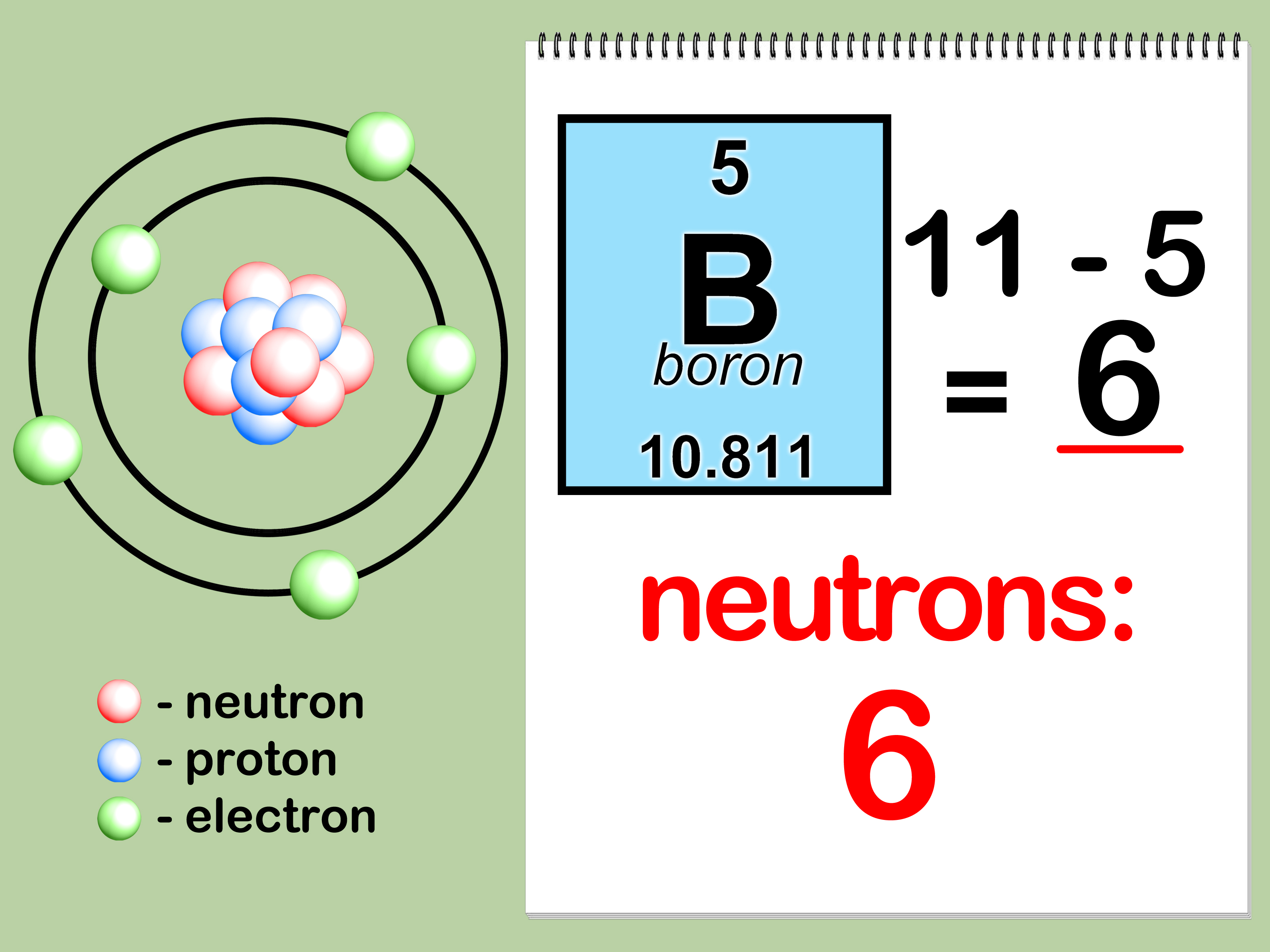
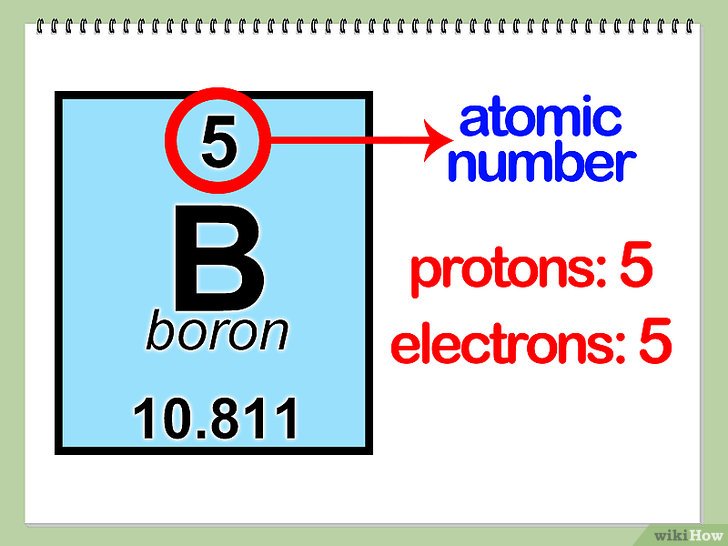
- Protonen: Bepalen welk element je hebt. Het aantal protonen is het atoomnummer.
- Neutronen: Dragen bij aan de massa van het atoom en beïnvloeden de stabiliteit van de kern. Verschillende aantallen neutronen leiden tot isotopen van hetzelfde element.
- Elektronen: Bepalen de chemische eigenschappen van het atoom, hoe het reageert met andere atomen en welke bindingen het vormt.
Zonder de juiste aantallen zouden de materialen om ons heen zich heel anders gedragen. Water zou misschien geen water zijn, ijzer zou niet roesten, en de zon zou geen energie produceren. De impact is enorm!
Real-World Impact: Medicijnen, Energie en Meer
De kennis over de aantallen protonen, neutronen en elektronen is cruciaal in talloze toepassingen:
- Medicijnen: De werking van medicijnen is afhankelijk van de manier waarop ze reageren met bepaalde moleculen in ons lichaam. Deze reacties worden bepaald door de elektronische structuur van de betrokken atomen, die weer afhankelijk is van het aantal protonen en elektronen. Neem bijvoorbeeld kankertherapieën. Sommige behandelingen zijn gericht op het verstoren van de DNA-structuur van kankercellen. Dit wordt bereikt door moleculen te gebruiken die selectief reageren met specifieke atomen in het DNA, gebaseerd op hun elektronische configuratie.
- Energie: Kernenergie is gebaseerd op het splijten van atoomkernen, waarbij enorme hoeveelheden energie vrijkomen. De stabiliteit van een atoomkern hangt af van de verhouding tussen protonen en neutronen. Kernreactoren gebruiken materialen zoals uranium-235, een isotoop met een specifiek aantal neutronen, om gecontroleerde kernsplijting te veroorzaken.
- Materialen: De eigenschappen van materialen, zoals hun sterkte, geleidbaarheid en magnetisme, worden bepaald door de manier waarop de atomen zijn gerangschikt en de interacties tussen hun elektronen. De ontwikkeling van nieuwe materialen, zoals supergeleiders en nanodeeltjes, vereist een diepgaand begrip van de atomaire structuur en de rol van protonen, neutronen en elektronen.
- Diagnostiek: Medische beeldvormingstechnieken zoals MRI (Magnetic Resonance Imaging) maken gebruik van de magnetische eigenschappen van atoomkernen, die afhangen van het aantal protonen en neutronen. Door magnetische velden te gebruiken, kunnen artsen gedetailleerde beelden van het lichaam verkrijgen en aandoeningen diagnosticeren.
Hoe Werkt Het: Een Eenvoudige Uitleg
Laten we het stap voor stap bekijken:
- Het Atoomnummer: Dit is het aantal protonen in de kern van een atoom. Elk element in het periodiek systeem heeft een uniek atoomnummer. Bijvoorbeeld, waterstof heeft 1 proton (atoomnummer 1), helium heeft 2 protonen (atoomnummer 2), en zuurstof heeft 8 protonen (atoomnummer 8).
- Massagetal: Dit is de som van het aantal protonen en neutronen in de kern. Omdat protonen en neutronen veel zwaarder zijn dan elektronen, bepaalt het massagetal grotendeels de massa van het atoom.
- Isotopen: Atomen van hetzelfde element kunnen verschillende aantallen neutronen hebben. Deze varianten worden isotopen genoemd. Bijvoorbeeld, koolstof-12 (12C) heeft 6 protonen en 6 neutronen, terwijl koolstof-14 (14C) 6 protonen en 8 neutronen heeft. Beide zijn koolstof, maar ze hebben verschillende massa's en eigenschappen.
- Elektrische Lading: Protonen hebben een positieve lading, elektronen een negatieve lading, en neutronen zijn neutraal. In een neutraal atoom is het aantal protonen gelijk aan het aantal elektronen, waardoor de totale lading nul is. Als een atoom elektronen verliest of wint, wordt het een ion en heeft het een positieve (kation) of negatieve (anion) lading.
Analogie: Stel je een voetbalteam voor. De protonen zijn de sterspelers (bepalen het team), de neutronen zijn de coaches (geven extra massa en stabiliteit), en de elektronen zijn de fans (bepalen de populariteit en interactie met andere teams). De samenstelling van het team bepaalt de prestaties en de interactie met andere teams.
Counterpoints: "Is Dit Echt Zo Belangrijk voor Mij?"
Sommige mensen argumenteren dat deze kennis alleen relevant is voor wetenschappers en onderzoekers. Ze vragen zich af of het echt nodig is voor de gemiddelde burger om de details van atoomstructuren te begrijpen.
Hoewel het waar is dat je niet dagelijks de exacte aantallen protonen, neutronen en elektronen hoeft te berekenen, is een basisbegrip van deze concepten wel degelijk waardevol. Het helpt je om:
- Wetenschappelijke informatie kritisch te beoordelen: Je bent beter in staat om nieuwsberichten over energie, medicijnen en milieu te begrijpen en te evalueren.
- Bewuste keuzes te maken: Bijvoorbeeld, bij het kiezen van voedingsmiddelen, materialen of technologieën.
- De wereld om je heen beter te begrijpen: Van de kleuren van een zonsondergang tot de werking van een smartphone, alles is gebaseerd op de interacties van atomen.
Bovendien is het belangrijk om te beseffen dat wetenschappelijke kennis niet alleen het domein is van experts. Een breder begrip van wetenschap bevordert innovatie, kritisch denken en een actieve deelname aan maatschappelijke discussies.
Oplossingen: Hoe Kun Je Je Kennis Vergroten?
Geen zorgen, je hoeft geen expert in kwantummechanica te worden om een beter begrip te krijgen. Hier zijn enkele manieren om je kennis te vergroten:
- Online bronnen: Er zijn talloze websites en video's die op een toegankelijke manier uitleg geven over atoomstructuren. Zoek bijvoorbeeld naar video's op YouTube of raadpleeg websites zoals Khan Academy.
- Boeken en artikelen: Er zijn veel boeken en artikelen die de basisprincipes van de scheikunde op een begrijpelijke manier uitleggen. Kijk in de bibliotheek of zoek online naar populair-wetenschappelijke publicaties.
- Cursussen en workshops: Overweeg het volgen van een korte cursus of workshop over scheikunde of natuurkunde. Veel volksuniversiteiten en online platforms bieden laagdrempelige cursussen aan.
- Experimenteren: Doe eenvoudige experimenten thuis om de principes van de scheikunde in de praktijk te ervaren. Bijvoorbeeld, onderzoek de reactie van azijn en baking soda om de principes van chemische reacties te begrijpen.
Conclusie
Het aantal protonen, neutronen en elektronen in een atoom is veel meer dan alleen een abstract wetenschappelijk concept. Het is de fundamentele basis van alles om ons heen. Door een basisbegrip te ontwikkelen van deze bouwstenen, kun je de wereld om je heen beter begrijpen, kritischer denken en bewuster keuzes maken.
Dus, ben je nu gemotiveerd om je kennis van atomen te verdiepen? Welke kleine stap ga jij vandaag zetten om meer te leren over de wonderen van de scheikunde?
Bekijk ook deze gerelateerde berichten:
- Hoe Lang Duurt Nederlands Examen Vwo
- Hoe Gaat Het In Het Frans
- Hoeveel Woorden In Het Nederlands
- Hoe Maak Je Een Goede Onderzoeksvraag
- Ds J Van Langevelde Zierikzee
- Hoeveel Ml Is 2 Liter
- Hoe Zet Je Examenstand Uit
- Hoe Doe Je Een X Opeen Ti-30xb Multiview
- Leren Schrijven Groep 3 Gratis
- Hoeveel Dagen Tot 13 Juli 2024
