Sterke Zuren En Basen Tabel
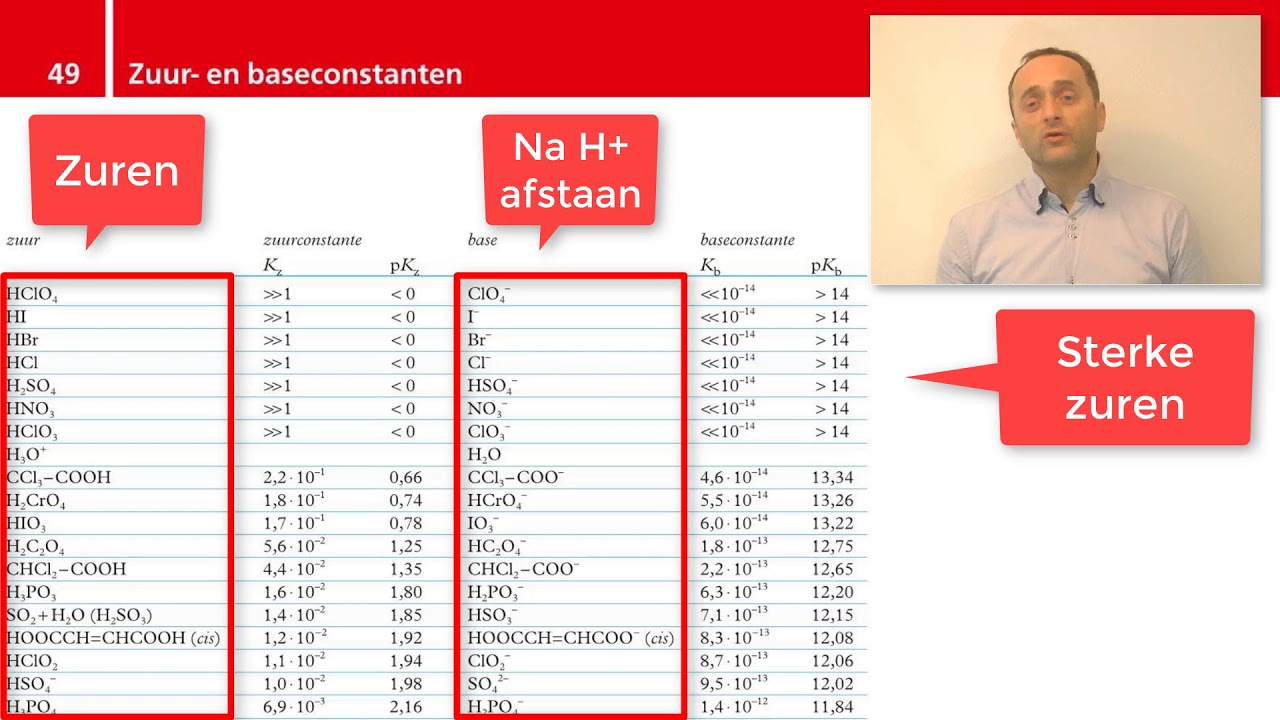
Ken je dat moment in de scheikunde les dat je verdwaald raakt in een zee van formules en termen? Zuren en basen, pH-waarden en neutralisatiereacties – het kan overweldigend zijn. Maar geen nood! Dit artikel is speciaal voor jou, of je nu een middelbare scholier bent die worstelt met scheikunde, een student die zijn kennis wil opfrissen, of gewoon iemand die nieuwsgierig is naar de wereld om hem heen. We gaan een essentiële tool in de scheikunde onder de loep nemen: de tabel met sterke zuren en basen. We ontrafelen waarom deze tabel zo belangrijk is en hoe je hem effectief kunt gebruiken.
Waarom een Tabel van Sterke Zuren en Basen?
In de scheikunde draait alles om reacties en interacties tussen stoffen. Zuren en basen spelen hierbij een cruciale rol. Sterke zuren en basen hebben de eigenschap om volledig te ioniseren in water, wat betekent dat ze alle beschikbare protonen (H+) afstaan (zuren) of protonen opnemen (basen). Dit volledige proces heeft een enorme invloed op de reactiesnelheid en de evenwichtsconstante.
Een tabel met sterke zuren en basen is dan ook onmisbaar, omdat deze je in één oogopslag laat zien welke zuren en basen volledig dissociëren in water. Zonder deze kennis zou je moeten vertrouwen op complexere berekeningen en veronderstellingen, wat de kans op fouten aanzienlijk vergroot. Met de tabel heb je een handig overzicht dat je direct kunt raadplegen, waardoor je tijd bespaart en nauwkeuriger kunt werken.
Denk bijvoorbeeld aan een titratie-experiment. Je moet precies weten welke sterkte je zuur of base heeft om de juiste hoeveelheid van de andere stof toe te voegen voor een volledige neutralisatie. De tabel helpt je om snel de juiste keuze te maken en je experiment succesvol uit te voeren.
Wat Staat er in de Tabel?
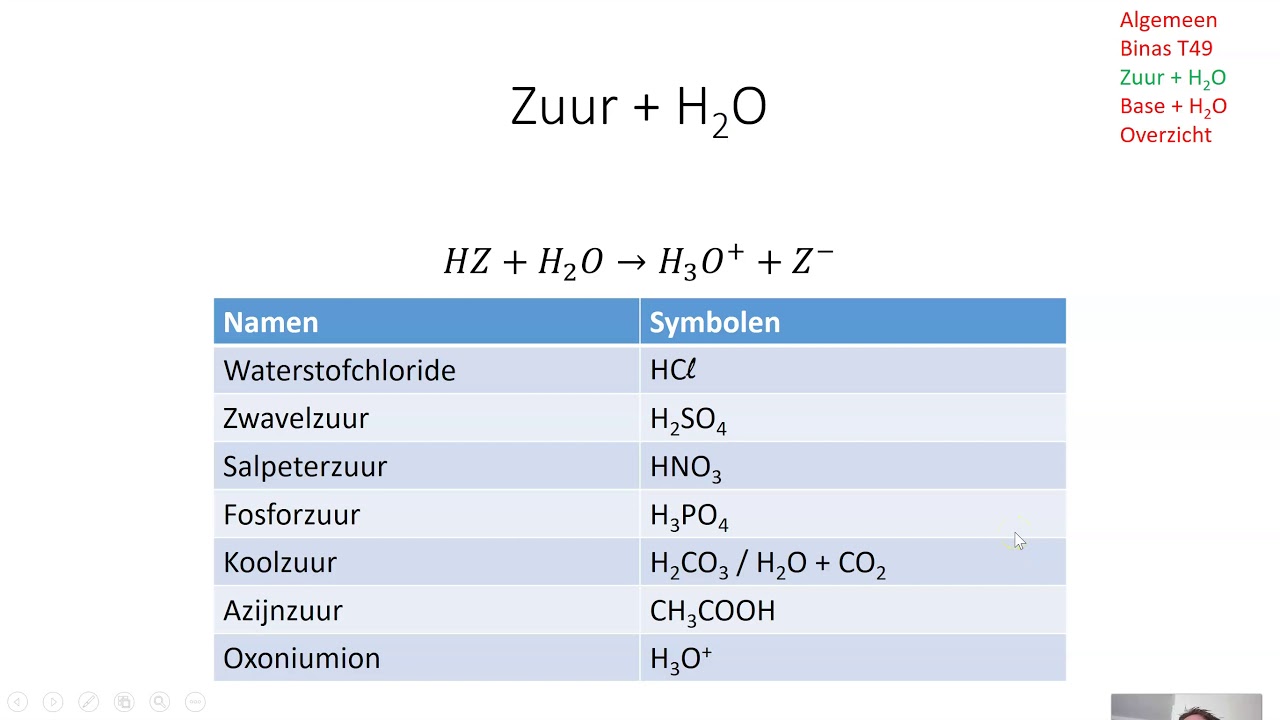
Een standaard tabel met sterke zuren en basen bevat doorgaans de volgende elementen:
- De formule van het zuur of de base: Bijvoorbeeld HCl (zoutzuur) of NaOH (natriumhydroxide).
- De naam van het zuur of de base: Zodat je de formule kunt koppelen aan de juiste term.
- De geconjugeerde base (voor zuren) of het geconjugeerde zuur (voor basen): Dit is het deeltje dat overblijft nadat het zuur een proton heeft afgestaan, of nadat de base een proton heeft opgenomen.
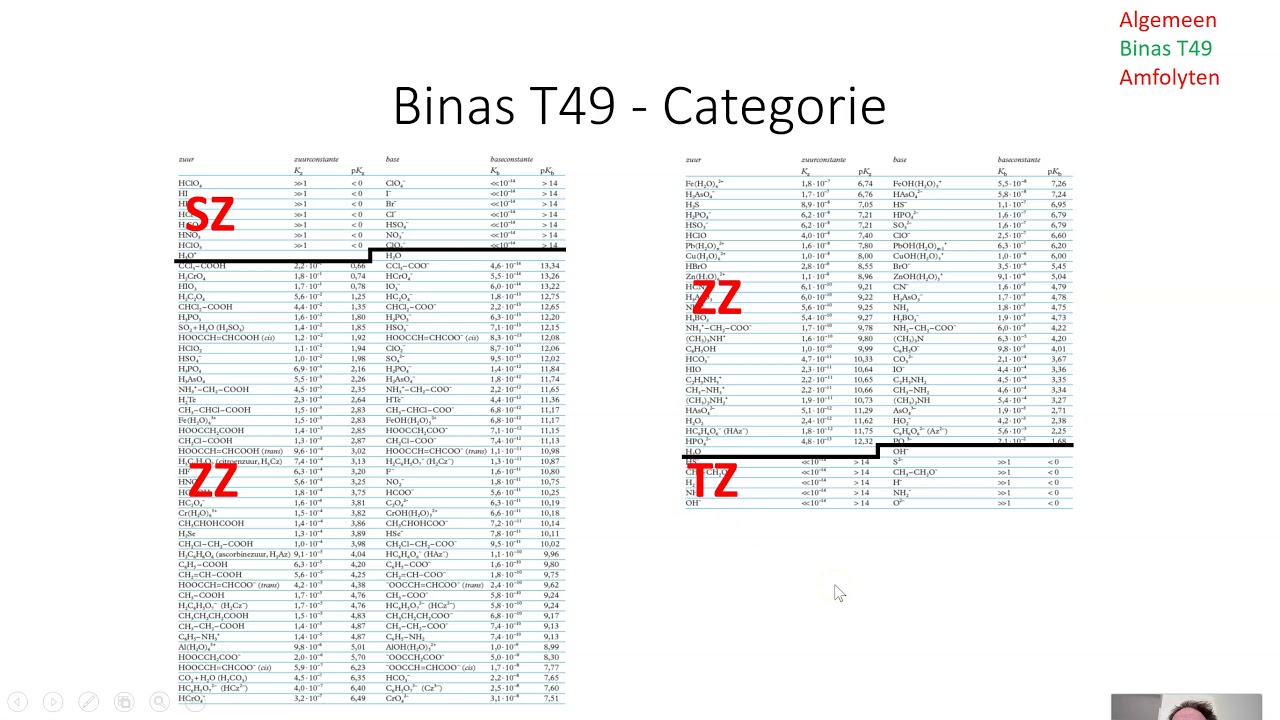
Het is belangrijk om te onthouden dat de tabel alleen de sterke zuren en basen bevat. Zwakke zuren en basen dissociëren slechts gedeeltelijk in water en vereisen andere methoden om hun sterkte te bepalen (zoals de zuurconstante Ka en de baseconstante Kb).
Voorbeelden van Sterke Zuren
Laten we eens kijken naar enkele veelvoorkomende sterke zuren die je in de tabel zult vinden:
- Zoutzuur (HCl): Een van de meest gebruikte zuren in laboratoria en industrie. Wordt ook gebruikt in maagzuur om voedsel af te breken.
- Zwavelzuur (H2SO4): Een krachtig zuur dat in veel industriële processen wordt gebruikt, zoals de productie van kunstmest.
- Salpeterzuur (HNO3): Gebruikt bij de productie van explosieven en kunstmest.
- Perchloorzuur (HClO4): Een zeer sterk oxiderend zuur, dat met de nodige voorzichtigheid moet worden behandeld.
- Broomwaterstofzuur (HBr): Een sterk zuur dat in organische syntheses wordt gebruikt.
- Joodwaterstofzuur (HI): Het sterkste halogeenwaterstofzuur.
Let op dat de concentratie van het zuur een rol speelt. Zelfs een sterk zuur kan een minder sterke werking hebben bij een lage concentratie.
Voorbeelden van Sterke Basen
Net als bij zuren zijn er ook een aantal bekende sterke basen:
- Natriumhydroxide (NaOH): Ook bekend als bijtende soda. Wordt gebruikt bij de productie van zeep, papier en textiel.
- Kaliumhydroxide (KOH): Vergelijkbaar met natriumhydroxide, maar wordt vaak gebruikt in batterijen en vloeibare zeep.
- Calciumhydroxide (Ca(OH)2): Ook bekend als gebluste kalk. Wordt gebruikt in de bouw en bij de behandeling van afvalwater.
- Bariumhydroxide (Ba(OH)2): Gebruikt in laboratoria voor titraties.
- Lithiumhydroxide (LiOH): Wordt gebruikt in de productie van smeermiddelen en batterijen.
De meeste sterke basen zijn hydroxiden van alkalimetalen (Groep 1) en aardalkalimetalen (Groep 2) in het periodiek systeem. Dit komt doordat deze metalen gemakkelijk een elektron afstaan, waardoor ze stabiele hydroxide-ionen vormen.
Hoe Gebruik je de Tabel Effectief?
Om de tabel optimaal te benutten, volg je deze tips:
- Ken de definities: Zorg dat je het verschil tussen een zuur, een base, sterk en zwak begrijpt.
- Oefen met voorbeelden: Los verschillende soorten problemen op waarbij je de tabel moet gebruiken. Denk aan neutralisatiereacties, pH-berekeningen, en het voorspellen van reactieproducten.
- Wees voorzichtig: Werk altijd veilig in het laboratorium, vooral bij het werken met sterke zuren en basen. Draag beschermende kleding, handschoenen en een veiligheidsbril.
- Combineer met andere kennis: Gebruik de tabel in combinatie met andere concepten, zoals de pH-schaal en bufferoplossingen, om een completer beeld te krijgen van zuur-basechemie.
- Raadpleeg je docent of bronnen: Als je ergens vastloopt, aarzel dan niet om hulp te vragen. Er zijn veel online bronnen en naslagwerken die je kunnen helpen.
Van Theorie naar Praktijk: Toepassingen in het Dagelijks Leven
Zuren en basen zijn niet alleen abstracte concepten in het laboratorium. Ze spelen een essentiële rol in ons dagelijks leven:
- Voedsel: Denk aan de citroenzuur in citroenen (zuur) of de natriumbicarbonaat (baking soda, base) die gebruikt wordt in gebak om het te laten rijzen.
- Reinigingsmiddelen: Veel reinigingsmiddelen bevatten zuren of basen om vuil en vet te verwijderen. Bijvoorbeeld, gootsteenontstoppers bevatten vaak natriumhydroxide (NaOH).
- Medicijnen: Sommige medicijnen zijn zuren of basen, en hun werking is afhankelijk van hun zuurgraad of basischheid.
- Landbouw: Boeren gebruiken zuren of basen om de pH van de bodem te reguleren, zodat gewassen optimaal kunnen groeien.
- Industrie: Zuren en basen worden gebruikt in tal van industriële processen, zoals de productie van kunststoffen, medicijnen en metalen.
Door te begrijpen hoe sterke zuren en basen werken, krijg je een beter inzicht in de wereld om je heen en de chemische processen die er plaatsvinden.
Conclusie
De tabel met sterke zuren en basen is een onmisbare tool voor iedereen die met scheikunde bezig is. Het biedt een snelle en gemakkelijke manier om te bepalen welke zuren en basen volledig dissociëren in water, wat cruciaal is voor het begrijpen en voorspellen van chemische reacties. Door de tabel effectief te gebruiken en te combineren met andere kennis, kun je je begrip van zuur-basechemie aanzienlijk verbeteren en je scheikundige vaardigheden naar een hoger niveau tillen. Dus, pak die tabel erbij, oefen, en ontdek de fascinerende wereld van zuren en basen! Onthoud altijd de veiligheidsvoorschriften bij het werken met deze stoffen.
We hopen dat dit artikel je heeft geholpen om de tabel met sterke zuren en basen beter te begrijpen. Ga nu aan de slag en pas je nieuwe kennis toe! Succes met je scheikunde avontuur!
Bekijk ook deze gerelateerde berichten:
- Ds Ten Voorde Nunspeet Afscheid
- Hoeveel Gram Is Een Eetlepel Roomboter
- Wat Doet Oestrogeen Met Je Lichaam
- Wat Is Een Genre Van Een Boek
- Peter R. De Vries Rinie Wielheesen
- Wat Is Een Goede Rentabiliteit
- Van Oude Mensen De Dingen Die Voorbij Gaan Samenvatting
- Jacob Veldhuyzen Van Zanten Kinderen
- Omrekenen Van Euro Naar Usd
- Avondgebed Voor Het Slapen Gaan
